最新氢气制备技术的研究进展
氢气是一种理想的二次能源,根据质量的不同,任何其他燃料在燃烧过程中释放的能量都低于氢释放的能量,CH4、汽油和煤的单位质量热值预计分别比H2低2.4、2.8和4倍。目前氢燃料电池已经少量应用于汽车领域,而且随着该产业的持续研究,在未来的人类生活中将会广泛应用。目前世界商用氢气的48%来自于化石燃料的裂解,醇类裂解制取的氢气占比30%,焦炉气制取氢气占18%,另外4%来自于电解水。日本由于化石燃料的匮乏以及环保水平较高,氢气的制取大部分来自于电解水,而我国化石能源充足,氢气大部分来自天然气的裂解和煤炉气的重整。地球上氢元素含量高,却大多以水的形式存在,难以直接利用。探索低成本、高效率、高纯度的大规模工业化制氢技术成为构建“氢社会”的基础。基于此本文对制氢领域取得的最新研究进展进行系统介绍。
1、氢气制备现状
目前,工业上常见的制氢的方法按照原料分类,可以将其分为:水分解制氢、有机物分解制氢、NH3分解、生物质制氢和硼氢化物催化水解制氢。
水分解制氢
水作为地球上最常见的资源,所蕴含的氢能不可估量,假如人类能够通过水来获取氢气,效益将是巨大的。根据制取方法不同,大致分为光催化水分解、电解水或电解海水等方法。
1972年Fujishima和Honda首先报道了TiO2半导体在光照条件下产生H2这一现象,而光催化效率经过数十年的研究得到了显著改善,但目前该技术的效率和稳定性依然无法满足工业化生产的标准,并且很少有人致力于研究可大规模的光催化制氢系统。常见的光催化水制氢的方法包括光电化学池、光助络合催化和半导体光催化。光催化水分解制氢的原理如下图所示,光照射到催化剂上发生诱导效应,由于光的能量大于催化剂禁带的禁阻,价带中的电子跃迁至导带,产生电荷,在价带中产生空穴,电荷参加还原反应生成氢气,空穴参加氧化反应生成氧气。光电化学电池法和光络合催化法是主要是吸收太阳光中的紫外光,但两者不同的是后者借助光敏剂可以提高对紫外光的吸收率,效率比光电化学电池法高出7%。这两种催化剂的价带过宽,只对紫外光产生响应,但太阳光中紫外光仅占3%,因此单靠这两种方法无法实现大规模的光催化制氢。半导体光催化主要因为其催化剂(包括:过渡金属氧化物、硫化物、氮化物、层状金属氧化物、复合层状物)价带低,尤其是某些非金属改性半导体(主要掺入N、F、C、S的阴离子)催化剂,可以显著降低其价带,扩展吸收光进入可见光范围内。邹松华等对TiO2半导体进行C修饰,对可见光的响应更强,提高了光子利用率和催化效率,是一种较为实用的方法。
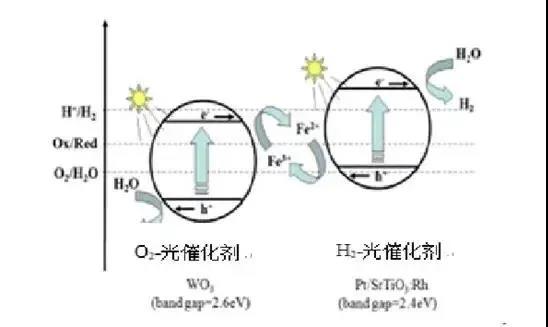
光催化水分解原理图
光催化水制氢主要存在的问题有(1)光能量损失,光催化过程中光经过一次能量浓缩器、反应器、反应溶液的过程易发生折射和吸收,太阳能无法被充分利用;(2)电荷重组,即电子对重新组合,在催化较慢的界面,易出现激发电荷的聚集,出现严重的电子重组问题,降低了氢气的生成效率;(3)多相催化环境反应中,反应物和产物转移引起的质量流障碍。分子和离子从大量的流体流到光催化反应位点,并经历扩散,接受电子后在催化剂表面产生氢气和氧气,气体通过成核和生长过程,造成界面催化反应慢,引起严重的逆反应并产生严重的能量流失,不利于氢气的生成;(4)催化剂的效率主要受其带隙和其接受光的类型影响,催化剂的灵敏度取决于其用于水分解的带隙能量,同时要保持还原和氧化电位必须保持在催化剂的带隙内才能发生光催化反应,能发生光催化的带隙能量必须处于1.23eV<Eg<3.26eV这个区间,因此需要研发一种带隙低、催化效率高的催化剂。
对于能量损失,应着重研究开发高效的浓缩器,减少光能的散失从而改善光的吸收。对于电荷重组,一般来说,为避免电荷发生重组,向水中加入一些牺牲试剂(如甲醇、乙醇等)或者某些电解质来改善光催化,另外某些掺杂其他金属(Pt、Au、Ag、Ni)的催化剂能明显实现电子对的空间分离,提高电子的接受能力。对于催化剂,目前开发窄带或转换光催化剂和某些良好的改性催化剂,以吸收更多的太阳能并解决电荷重组的问题。对于质量流的的障碍,应研究电子的转移行为,防止高电荷在催化剂表面的富集,促使反应逆向进行,着重研究催化剂界面传质和产物转移,以便增大氢气的产率。
有机物制氢
有机物制氢在我国工业制氢中占有很大的比重,有机物种类繁多,因此利用有机物制氢气的原料和方法多种多样,利用化石能源裂解制氢和醇类重整制氢,是工业上很常用的制氢手段。
化石能源制氢
化石能源中主要用作制氢原料的有炼厂干气、天然气、煤、轻石脑油和重油等。
天然气的主要成分为甲烷,在甲烷制氢的众多方法中,甲烷水蒸气重整工艺较为成熟,但其成本高、能耗高。而甲烷催化裂解制氢耗能少,产物中不含COX,产物纯度较高,相对效果较好。
工业水煤气变换催化反应也被称为水汽变换(WGS),最初反应用于从H2流中去除CO。该法被广泛用于以煤、石油、天然气及醇类为原料的制氢工业,调整合成气的H2O/CO比或将大量的一氧化碳转变为二氧化碳,经后续的分离手段制备纯度相对较高的氢气。该反应需要在合适的催化剂和一定温度的条件进行。水汽变换反应能够同时制取氢气并净化一氧化碳。
甲醇重整制氢
甲醇制氢具有反应温度低、原料来源广泛、能耗低、便于运输等优势。传统甲醇制氢方法主要包括甲醇裂解(SD)、甲醇水蒸气重整(SMR)、甲醇部分氧化(POM)和甲醇自热重整(ASRM)等,这些制氢技术大多可实现工业化制氢。甲醇裂解直接转化为H2和CO,甲醇水蒸气重整制氢(SMR)通过一种甲醇和水蒸气反应制氢的方法,该方法在能耗方面具有较大优势,但因反应温度下所需催化剂的限制,目前仅适合中小规模制氢。
氨催化分解制氢
氨催化分解制氢是一种绿色环保的技术,但通过氨的分解制备氢气,转化效率相对较低。在目前研究中,通过加入铁基、钌基、镍基、过渡金属氮化物及碳化物等催化剂,会使得氨的催化效率增加。其中,钌基有很高的催化活性,尤其是用碳纳米管(CNTs)作为载体,由于CNTs具有良好的导电性,降低Ru离子电势,从而有利于从Ru表面脱出吸附的氢。铁基催化剂来源丰富、成本较低,但其与镍基和钌基催化剂相比活性较低。镍基催化剂从成本和活性考虑是一种应用前景较好的催化剂,但需要在较高的温度下反应,这会使得催化剂的活性降低。
生物质制氢
生物质是一种可再生能源,具有巨大的能源生产潜力。生物质制氢可以通过暗发酵或光发酵途径实现。下图为生物质制氢的原理图。由于生物质制氢技术尚不成熟,目前还未实现应用。另外,生物质的氢含量非常低,导致生物质产生的氢气产量较低。生物质制氢中约50%的氢是在水裂解过程中通过蒸汽重整反应产生的。该工艺对原料的能量含量有固有限制。
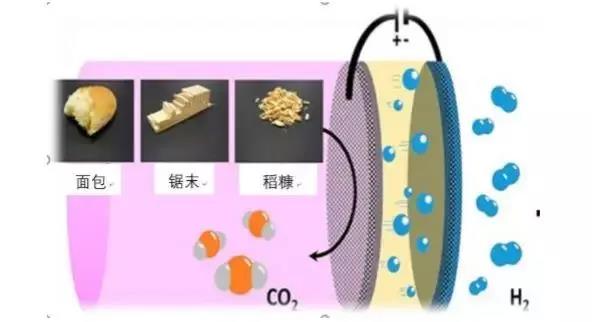
生物质制氢原理图
硼氢化物制氢
硼氢化物具有储氢密度大、产氢纯度高、储存运输安全、反应易控制、产物可回收循环等优点,硼氢化物制氢这也是未来制氢的一种手段。但这种方法制氢反应所需活化能较高,需要用催化剂降低它的反应活化能。目前的催化剂主要有硼氢化物负载型金属催化剂和非负载型金属催化剂。负载型金属催化剂是将金属催化剂附着在石墨烯等固体上,以便控制反应速率和催化剂的回收利用;非负载型金属催化剂一般为粉末状,包括贵金属和多元非贵金属催化剂。这两种催化方法都存在催化剂失活的问题,未来这方面的研究方向主要是合成贵金属与非贵金属复合催化剂、多元金属催化剂、新型载体的制备以及研究催化剂失活的机理,以此来提高催化剂活性,解决催化剂失活的问题。
2、电解水制氢
电解水制氢的成本较高,目前该技术制氢量占我国氢气总产量的一小部分。水电解制氢技术根据电解质种类的不同,可以分为碱性电解水制氢、质子交换膜(PEM)电解水制氢及固体氧化物电解水制氢等技术。
碱性电解水制氢
碱性电解水制氢是一种成熟的制氢技术,已广泛应用电力、电子等工业领域。下图为碱性电解水的示意图,由阳极、阴极、电源、隔膜、电解质溶液组成,电解质溶液通常为20%~30%的NaOH或KOH的溶液。电极一般为镍电极。碱性电解技术的优点是不需要昂贵的催化剂,且寿命较长,其使用寿命可超过10年。
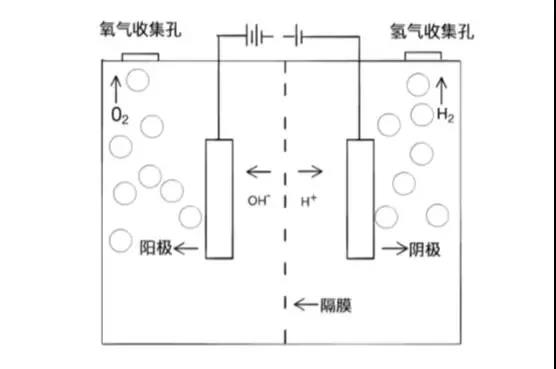
碱性电解水的示意图
碱性电解水制氢技术主要存在的问题是液体电解质中高欧姆损耗而产生的低电流密度,整个碱性电解水系统中,电阻主要来自于三个方面:外电路电阻、传输电阻、电化学电阻。其中传输电阻是造成高欧姆损耗的主要原因,传输电阻是指电解过程中所造成的电阻,如在电极表面生成的气泡、用于分离H2、O2的隔膜均会对电子的传导产生影响。针对高欧姆能耗,可以采用通过电解质循环或通过改变电极表面性质或者加入惰性表面活性剂,加速气泡的逸出,另外可以开发新型隔膜替代现有隔膜,降低隔膜电阻。
质子交换膜电解水制氢
与碱性水电解相比,PEM技术显著减小了电解槽尺寸和重量。PEM电解采用的质子交换膜既是离子传导的电解质,又起到隔离气体的作用。PEM技术的电解电流密度比碱性电解技术高,且产生的氢气纯度比碱性电解水的纯度也高。图4为PEM电解水的原理图,水通入阳极区并氧化为氧气,质子以水合质子形式通过质子交换膜在阴极还原为氢气。阳极和阴极主要为贵金属催化剂,如阳极为金属铱,阴极为金属铂。
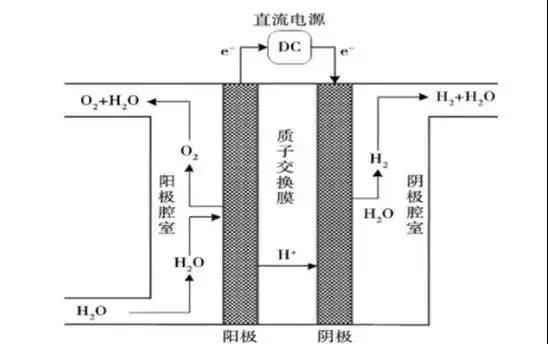
PEM电解水原理图
PEM的问题主要在于成本高。RuO2和IrO2一般为PEM电解阳极的优级催化剂,Pt被认为是氢析出反应的基准电催化剂,这些贵金属的高成本阻碍了PEM的发展及规模化应用。另外,质子交换膜的造价也较为昂贵,且这种交换膜在使用过程中会发生降解,缩短膜的寿命。目前,针对膜的使用寿命问题还未找到明确的解决途径,针对贵金属催化剂,目前主要通过降低催化剂载量和开发合金催化剂等途径降低催化剂部分的成本。
高温固体氧化物电解水
固体氧化物电解水的工作温度在700~1000℃,由于反应的高温致使该技术的效率比碱性电解水和PEM电解水的效率更高。该技术电解质主要为固体氧化物,通常为Y2O3、ZrO3,其反应过程是水在阴极接受电子产生氢气和O2-负离子,O2负离子通过电解槽传导至阳极产生O2。固体氧化物电解水技术目前处于开发阶段,研究和重点在于提高陶瓷材料在高温下的耐久性。
下表为三种水电解技术的指标对比。可以发现,碱性电解水技术具有使用寿命长的优点,但电解质使用的KOH或者NaOH溶液会污染环境,该技术电流密度也较低。PEM电解水具有电流密度大、氢气纯度高等优点,安全性和操作简便性也较好,但由于成本等原因,目前仅适用于小规模的氢气生产。高温固体氧化物电解技术系统效率高于另外两种技术,但其工作温度过高,目前仍处于研究阶段。
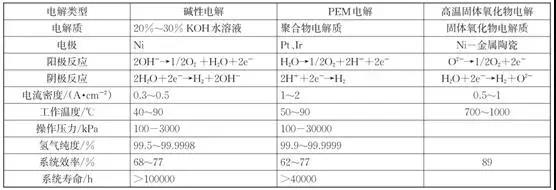
电解水方法的比较
3、结语
现阶段工业制氢主要依靠化石能源的重整,其环境和产率弊端不容忽视。以水为原料制取氢气,相比而言更清洁且原料廉价易得。随着光解水和电解水制氢的不断进展,给未来制氢引领了一条更加友好的道路。
光催化水制氢目前还处于研究阶段,需要在高效催化剂开发、提高能量利用效率等方面深入工作。对于电解水制氢来说,碱性电解水是现阶段最廉价的电解制氢方式,但其能量利用效率并不理想。PEM电解水制氢技术由于其电解槽的耐久性和成本问题,目前无法大规模使用,需要进一步研究适应长期生产的材料。



